私たちの主な研究内容

細胞生物学:
Cell Biology
① がん特異的な細胞質タンパク質分泌機構
・分子機構の解明(CUPSの発見)
・発がん・がん進展との関係解明
・強皮症との関係解明
② 細胞膜タンパク質の核移行機構の解明
・細胞膜―核間移行機構の解明
・血管内皮細胞と強皮症との関係解明
細胞生物学: Cell Biology
がん特異的な細胞質タンパク質分泌機構
〜 分子機構の解明(CUPSの発見)と、発がん・がん進展との関係解明 〜
我々のチームは、がん細胞株の培養上清(細胞外成分)を用いて、型破り分泌される細胞内タンパク質を網羅的に探索しました。その結果、従来は細胞質や核などに存在するタンパク質が肝がん細胞株の培養上清から数多く検出されることがわかりました。このうちリン酸化酵素PKCδが複数の肝がん細胞株の培養上清において高頻度に検出される一方で、正常の肝細胞や他のがん細胞株の培養上清ではほとんど検出されないことを突き止めました。
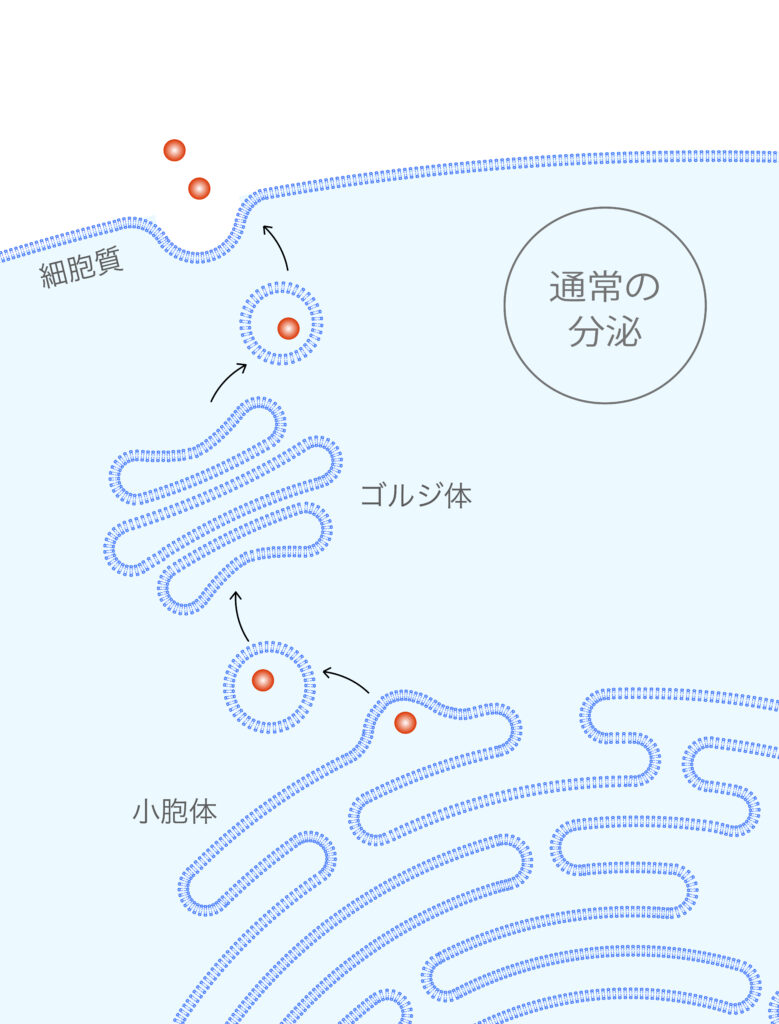
我々のチームは、PKCδ分泌の機能的特徴も明らかにしています。まず細胞傷害の程度を調べる検査マーカーである乳酸脱水素酵素(LDH)を用いて解析したところ、PKCδの細胞外分泌は生きた細胞に由来しており、LDHの細胞外漏出とは明らかに細胞外に出ていくタイミングが異なっていることがわかりました。そして、一般的な分泌タンパク質は、合成時に作られる分泌シグナルに依存して、小胞体内に入った後、ゴルジ体を通して細胞外に分泌される一方で、PKCδは、分泌シグナルを持たない細胞外分泌、いわゆる型破り分泌(CUPS)をする事を見出しました。
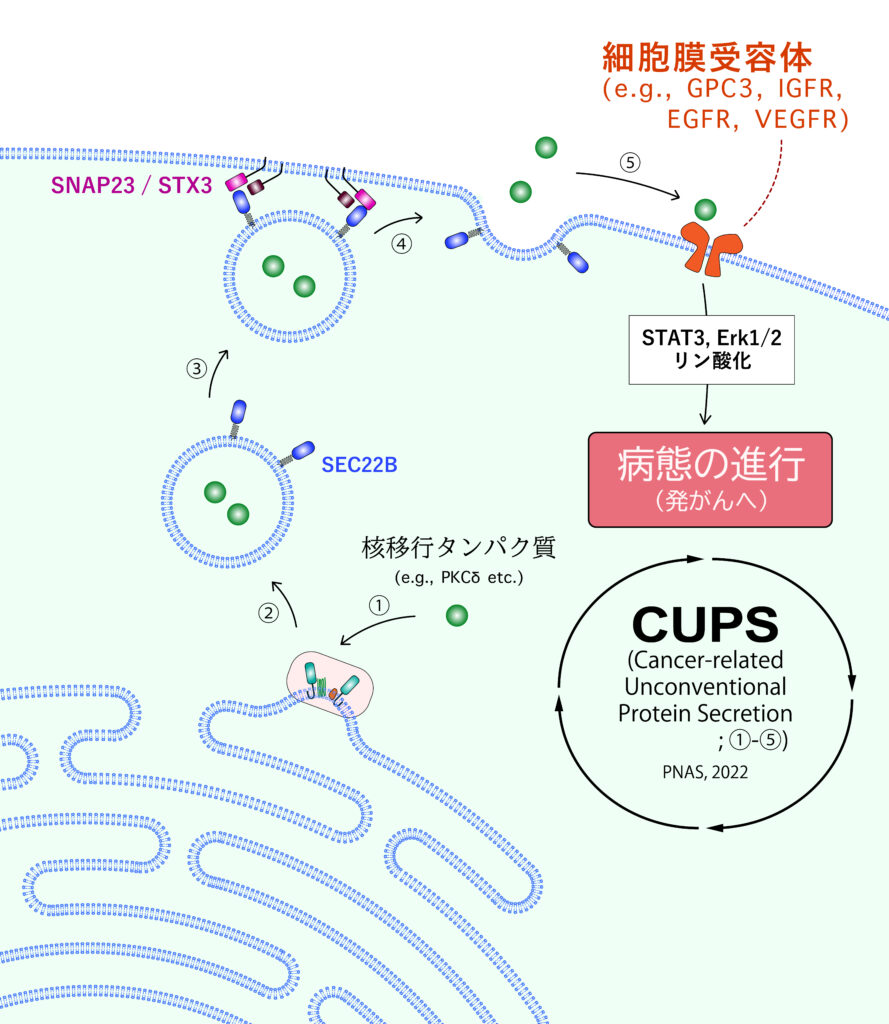
次にPKCδの細胞外分泌と肝がん病態との関係を調べるために、細胞外PKCδの機能解析を行いました。その結果、分泌されたPKCδが肝がん細胞に発現するグリピカン3と呼ばれる細胞表面タンパク質と結合し、細胞増殖に関わるシグナル伝達系を活性化させていることを突き止めました。さらに、PKCδのモノクローナル抗体を用いて、細胞外でのPKCδ機能を中和したところ、肝がんの腫瘍形成能が明らかに阻害されることがわかりました。これらの結果は、PKCδ分泌が肝腫瘍の増大に積極的に関わっていることを示唆しているだけでなく、抗体療法の有望な標的になる可能性が示されました。
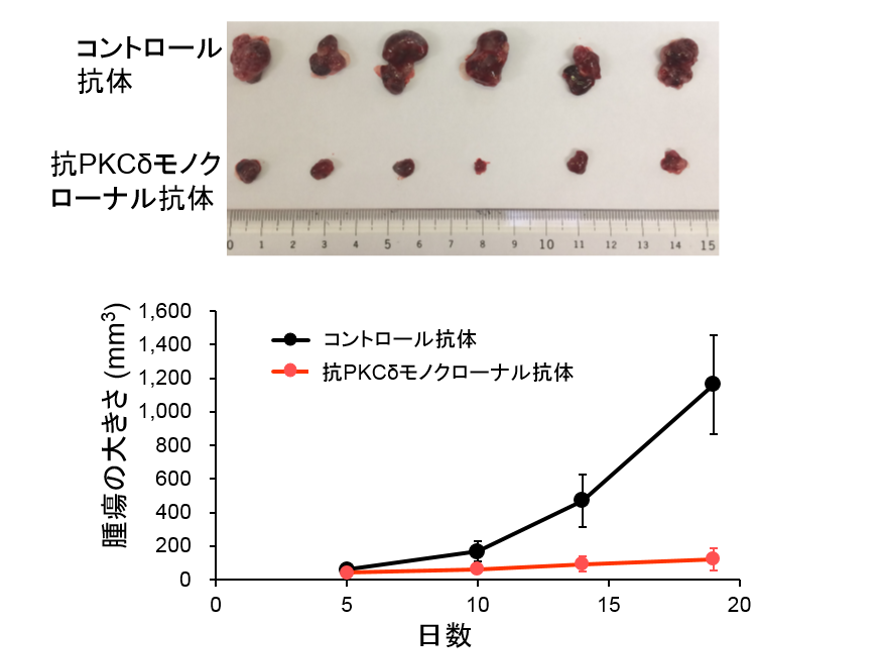
抗PKCδモノクローナル抗体を投与した群ではコントロール抗体の投与群と比べて、
明らかに腫瘍が小さい。
病態研究: Related Diseases
血中PKCδを標的とした早期肝がんバイオマーカー開発
現在、臨床で主に使用される肝がんの腫瘍マーカーであるAFPやPIVKA-IIは、いずれもがんの病期が進むにつれて上昇するものの早期には陽性にならず、それらの感度は早期診断のためには満足のいくレベルではありません。また腫瘍マーカー陰性となる症例が約20 %も存在します。特に近年増加傾向にある非アルコール性脂肪肝炎 (NASH) 肝がんではウイルス性肝がんと比べ既存の腫瘍マーカーの陰性率が高いことが知られ、ウイルス性とは異なる肝がんサーベイランス法が確立していないことから巨大かつ進行がんで発見されることが少なくないのが現状です。これらの腫瘍マーカー陰性患者では定期的サーベイランス以外での肝がん精査に必須である画像検査を施行する機会が失われ、結果として早期発見されず進行がんで発見される症例が多数存在することが問題となっていました。
我々は、肝がんのなかでも約90%以上を占める肝細胞がん(HCC)診断において、新規バイオマーカーとしての血清PKCδの有用性を検証しました。
健常人、慢性肝疾患患者、治療前HCC患者の血清PKCδをサンドイッチELISA法で測定し、HCCの診断能を解析するとともに既存マーカーであるAFP/PIVKA-II と比較検討しました。
HCC群の血清PKCδは、健常人や慢性肝疾患患者群 (慢性肝炎や肝硬変患者) と比較して有意に高値でした。血清PKCδのHCC診断能は、既存の腫瘍マーカーと同程度であることが判明しました。またPKCδはAFP/PIVKA-IIと相関はなく、既存マーカーとは異なる特性を有すると考えられました。さらに、既存マーカーとの組み合わせによりHCC診断能が向上することが示されました。
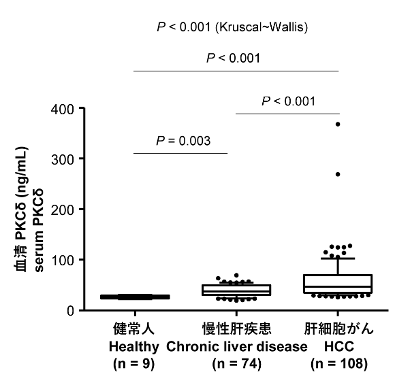
血清PKCδ値分布
さらに特筆すべきは、単発かつ最大腫瘍径20mm以下HCC群 (BCLC stage 0; very early stageに相当)では、PKCδの陽性率は45.0%と最も感度が高いことです。一方で既存マーカーであるAFP、PIVKA-IIの陽性率はそれぞれ15%にとどまり、AFPとPIVKA-IIを組み合わせて用いてもPKCδの診断能を超えることはありませんでした。従って、血清PKCδを用いることで、これまで早期診断が困難であった症例を拾い上げることが可能になる可能性があると考えます。
血清PKCδはHCCで特異的に高値であり、既存マーカーを相補的に補完するだけでなく、早期発見が困難な既存マーカー陰性症例や早期HCC患者を特定できる新規診断バイオマーカーとしての有用性が示され、肝がんの予後の向上が期待されます。
我々が血清PKCδ測定に用いたサンドイッチELISAキットは研究用試薬であり、今後実臨床での測定を実現するための診断キットの開発を目指しています。(国立研究開発法人日本医療研究開発機構(AMED)革新的がん医療実用化研究事業「早期肝がんに対するPKCδを用いた新規高感度診断法の開発(研究開発代表者:山田幸司)」で、研究が進行中です。)
また、我々のグループが同定した肝がんの新規早期診断マーカーPKCδと肝がん患者の臨床的特徴との関連性を解析することにより、血清PKCδ測定が将来、肝がん抑止や予後向上のための早期診断のみならず、予後予測や治療反応性バイオマーカーとなる可能性を多施設共同研究で検証する予定です。
創薬研究: Translational Research
オルガネラ創薬へのアプローチ
我々の強みである基礎研究と病態研究を、研究で終わらせない。実際に臨床の場で使える形にすることで、人類にいち早く還元する。ここにスピード感を持って取り組んでいます。慈恵会医科大学から国内、グローバルに展開し、様々な分野での人類貢献を目指しています。


検査薬の開発や創薬は、我々のチームだけでは遂行できません。多くの企業にスポンサーやサポーターとなって頂き、様々な分野の皆様の力をお借りして、一歩ずつ研究を前に進めております。